Einleitung
Im vorliegenden Fall handelt es sich um einen Zucht- und Mastbetrieb mit 600 Sauen in Nordirland, der innerhalb eines Jahres auf 1.000 Sauen anwuchs.

Die benutzten Impfpläne sind in Tabelle 1 dargestellt.
Tabelle 1: Impfplan.
| Impfstoff | Jungsauen | Sauen | Eber | Ferkel |
| Parvovirus | Injektion von 2 ml bei der Selektion | Injektion von 2 ml 2 Wochen nach dem Abferkeln | Injektion von 2 ml zweimal pro Jahr | |
| Erysipel | Injektion von 2 ml bei der Selektion und 2 Wochen vor der Deckung | Injektion von 2 ml 2 Wochen nach dem Abferkeln | Injektion von 2 ml zweimal pro Jahr | |
| Colibacillose & Clostridiose | Injektion von 2 ml 6 und 2 Wochen vor dem Abferkeln | Injektion von 2 ml 2 Wochen vor dem Abferkeln | ||
| PRRS (MLV) | Injektion von 2 ml bei der Selektion und 60 Tage nach der Deckung | Injektion von 2 ml 6 Tage nach dem Abferkeln und 60 Tage nach der Deckung | Injektion von 2 ml zweimal pro Jahr | |
| PCV-2 | Injektion von 1 ml beim Absetzen | |||
| Enzootische Pneumonie | 1 ml im Alter von 10 - 14 Tagen und beim Absetzen |
Die Jungsauen werden im Betrieb selbst gezüchtet. Eber dienen der Stimulierung. Jungsauen und Sauen werden mit Samen aus einem einzigen Zuchtbetrieb künstlich besamt.
Der nächste Schweinebetrieb ist 2 km entfernt.
Verlauf
Der Landwirt kontaktierte den Tierarzt aufgrund zunehmender Atemnot und der Verschlechterung des Körperzustands, einhergehend mit einem Anstieg der Mortalität bei Absetzferkeln und Mastschweinen.
Untersuchung
Klinische Untersuchung
Bei einem Besuch des Betriebs im September 2017 gab es viele 6 bis 15 Wochen alte Ferkel mit klinischen Anzeichen einer Verschlechterung des Körperzustands und abdominaler Hechelatmung (Abb. 1 & 2). Husten trat nur in geringem Maß auf. Die Buchten waren überbelegt.

Abbildung 1: Absetzferkel in überbelegten Buchten mit einigen Tieren, die klinische Symptome einer Verschlechterung ihres Körperzustands zeigen.

Abbildung 2: Tiere, die klinische Symptome einer Verschlechterung ihres Körperzustands zeigen
Nach Auskunft des Landwirts lag die Mortalität von der Ferkelaufzucht bis zur Mast zwischen 3,5 - 5 %. Allerdings entsprachen diese Mortalitätsraten absolut nicht denjenigen, die auf den wöchentlichen Anschlagtafeln im Betrieb aufgeführt waren (Abb. 3).
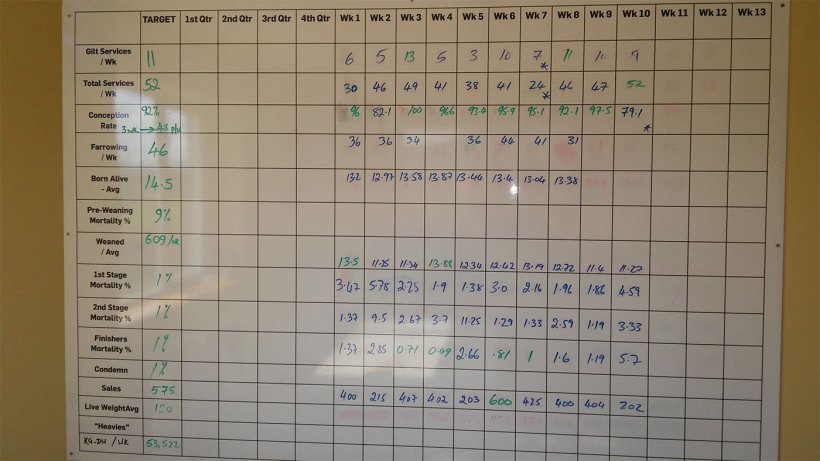
Abbildung 3: Wöchentliche Leistungen des Betriebs bis September 2017
Laut Anschlagtafel betrug die Mortalität von der Ferkelaufzucht bis zur Mast in den letzten 10 Wochen 8,48 %. Die Mortalität lag in der 1. Phase (Alter von 4 bis 9 Wochen) bei 2,64 %, in der 2. Phase (Alter von 10 bis 15 Wochen) bei 3,82 % und bei den Mastschweinen (Alter von 16 Wochen bis zur Schlachtung) bei 1,83 %.
Laboruntersuchungen
Zwei 6 Wochen alte Absetzferkel mit abdominaler Hechelatmung und Verschlechterung des Körperzustands wurden eingeschläfert, um anschließend im Betrieb seziert zu werden (Abb. 4 & Video 1). Die entnommenen Proben wurden dem Labor zur Analyse übergeben.

Abbildung 4: Absetzferkel mit Atemnot und Gedeihstörung.
Video 1: Absetzferkel mit Atemnot und Gedeihstörung
Die Ergebnisse der Sektion und der Laboruntersuchungen sind in Tabelle 2 zusammengefasst. Die Abbildungen 5, 6, 7 und 8 zeigen die fotografisch festgehaltenen Ergebnisse der Sektion.
Tabelle 2: Laborergebnisse der beiden 6 Wochen alten Absetzferkel.
| Absetz-ferkel | Sektion | Bakteriologischer Befund | Biomolekularer Befund | Histologischer Befund |
| 1 | Schlechter Körperzustand, Untergewicht, Perikarditis, Pleuritis, Konsolidierung der Lunge im ventralen Bereich des Herz- und des Zwerchfelllappens mit interstitieller Pneumonie. |
Pasteurella multocida (Lunge) Streptococcus suis Serotyp 3 (Lunge). |
Negativ auf Mycoplasma hyopneumoniae, IInfluenzavirus-Typ A & PVC-2 durch RT-PCR (Lunge). EU-PRRS-positiv durch RT-PCR (Ct-Wert: 21,2) mit Lunge von Absetzferkeln 1 und 2. |
Bronchien mit neutrophilen Granulozyten und Hyperplasie des Bronchialepithels. Das Lungengewebe zeigt die verschiedenen Stadien einer fibrinösen Bronchopneumonie. Folglich sind häufig Hepatisation und Karnifikation feststellbar. Die Proliferation von fibrösem Gewebe tritt multifokal in den interlobulären und den interalveolaren Räumen auf. Diese Befunde sind charakteristisch für eine chronische Entzündung. |
| 2 | Schlechter Körperzustand, Untergewicht, vergrößerte Lymphknoten in der Leistengegend, Perikarditis, Pleuritis, Konsolidierung der Lunge im ventralen Bereich des Herz- und des Zwerchfelllappens mit interstitieller Pneumonie. |
Pasteurella multocida. (Lunge). | Negativ auf Mycoplasma hyopneumoniae, Influenzavirus-Typ A & PVC-2 durch RT-PCR (Lunge) EU-PRRS-positiv durch RT-PCR (Ct-Wert: 21,2) mit Lunge von Absetzferkeln 1 und 2. |
Die Lunge weist Anzeichen einer chronischen Entzündung auf. Die Entzündung gehört eher zum katarrhalisch-eitrigen Typ. Die Bronchien sind voller neutrophiler Granulozyten und das Bronchialepithel ist hyperplastisch. Die Chronizität ist gekennzeichnet durch die Proliferation von fibrösem Gewebe in den interstitiellen Räumen. Die Pleura ist fokal hyperplastisch und feststellbar ist ein interstitielles Ödem. |
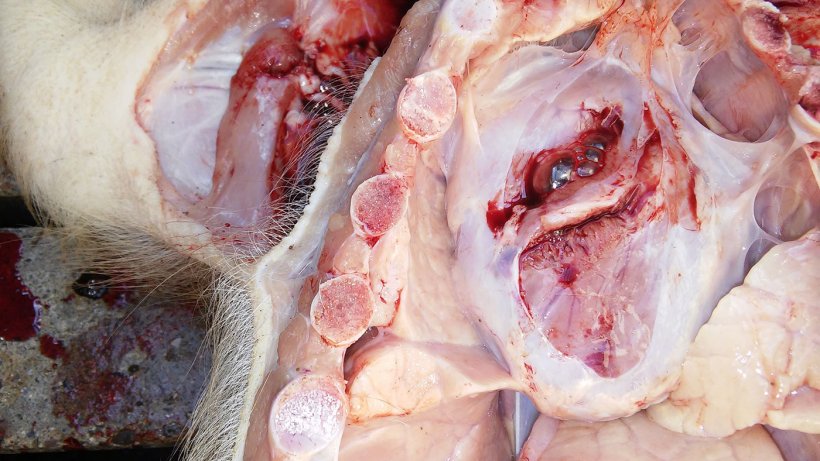
Abbildung 5: Perikarditis
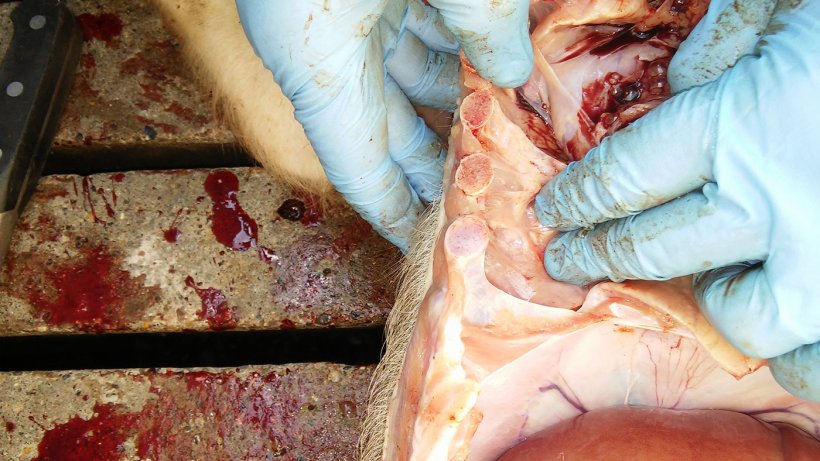
Abbildung 6: Pleuritis zwischen Lungenfell und Brustfell
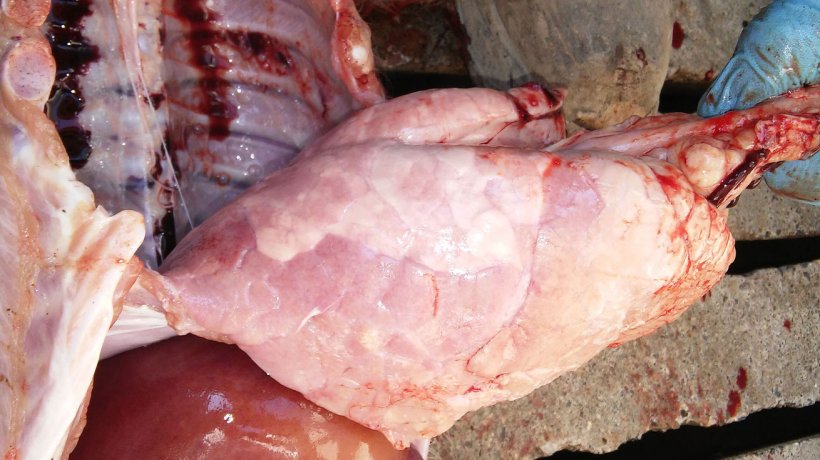
Abbildung 7: Interstitielle Pneumonie mit ausgeprägter Lungenkonsolidierung des ventralen Zwerchfelllappens.
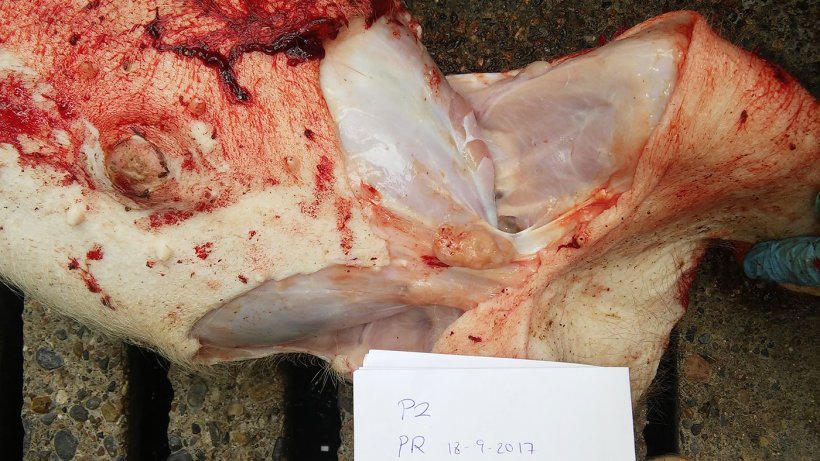
Abbildung 8: Vergrößerter mesenterischer Lymphknoten
Differentialdiagnose
Auf Grundlage der klinischen Untersuchungen und der Laboruntersuchungen wurde die folgende Liste der Differentialdiagnosen erstellt:
- PRRS (Porcines Reproduktives und Respiratorisches Syndrom)
- PCV2 (Porcines Circovirus Typ 2)
- Influenzavirus Typ A
- Enzootische Pneumonie (Mycoplasma hyopneumoniae)
Aufgrund negativer Laborergebnisse wurden virale Krankheitserreger wie z. B. Influenzavirus Typ A und PVC-2 ausgeschlossen. Die Impfpläne gegen PVC-2 waren in diesem Betrieb zufriedenstellend.
Enzootische Pneumonie wurde aufgrund negativer Laborergebnisse, zufriedenstellender Impfprogramme und nicht auftretendem Husten im Mastbetrieb ausgeschlossen.
Aufgrund der Vorgeschichte und der einheitlichen Ergebnisse der klinischen und der Laboruntersuchungen liegt die Diagnose einer PRRS-Infektion mit sekundärer opportunistischer bakterieller Infektion im Mastbetrieb nahe.
Programm zur Bekämpfung
Es wurde vorgeschlagen, alle Ferkel im Alter von 10 – 14 Tagen mit einem modifizierten Lebendimpfstoff gegen PRRS zu impfen.
Reaktion auf das Programm zur Bekämpfung
Die Atemnot und Gedeihstörungen bei den Schweinen verringerten sich. Die Mortalität sank drei Monate später deutlich auf 5,2 %. Die Mortalität lag in der 1. Phase (Alter von 4 bis 9 Wochen) bei 2,25 %, in der 2. Phase (Alter von 10 bis 15 Wochen) bei 1,72 % und bei den Mastschweinen (Alter von 16 Wochen bis zur Schlachtung) bei 1,24 % (Abb. 10). Die Besatzdichten wurden dabei nie geändert..
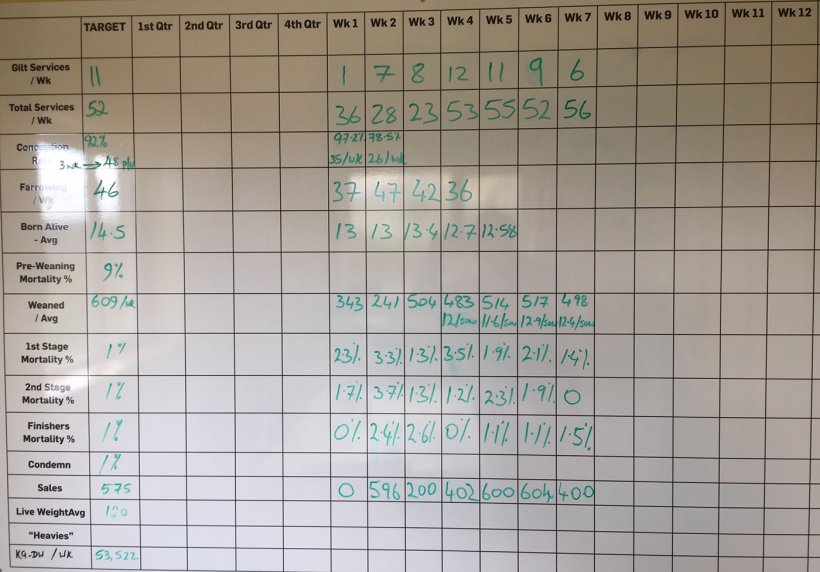
Abbildung 10: Wöchentliche Leistung des Betriebs bis Februar 2018
Diskussion
In den späten 1980er Jahren wurden in den Vereinigten Staaten schwere Reproduktions- und Atemwegserkrankungen beschrieben (Keffaber 1989). Der Krankheitserreger war damals unbekannt. Das gleiche Syndrom wurde 1990 in Deutschland beschrieben (OIE 1992). Der Krankheitserreger wurde erstmals 1991 in den Niederlanden (Wensvoort et al. 1991) isoliert und Porcines Reproduktives und Respiratorisches Syndrom (PRRS) genannt (Terpstra et al. 1991).
PRRS-Infektionen wurden erstmals 1997 in Nordirland (Anonym, 1997) und 1999 in Irland (Ohlinger et al., 2000) festgestellt.
PRRS tritt mit wenigen Ausnahmen in den meisten schweineerzeugenden Ländern der Welt auf. Länder wie Schweden (Carlsson et al. 2009), Norwegen (OIE 1997), Finnland (Bøtner 2003), die Schweiz (Corbellini et al. 2006), Neukaledonien (OIE 1996), Neuseeland (Motha et al. 1997), Australien (Garner et al. 1997), Argentinien (Perfumo und Sanguinetti 2003), Brasilien (Ciacci-Zanella et al. 2004) und Kuba (Alfonso und Frias Lepoureau 2003) sind offiziell frei von PRRS.
Die Schwere einer PRRS-Infektion variiert von Betrieb zu Betrieb. Nichtinfektiöse Faktoren verschärfen die Ausprägung klinischer Symptome. Zu diesen nichtinfektiösen Faktoren zählen das Betriebsmanagement, die Umstallungen, die Unterbringung und die Temperaturregelung (Zimmerman et al. 2012). Infektionen, die gleichzeitig mit anderen viralen und bakteriellen Erregern auftreten, verstärken oder verschlimmern die Schwere der klinischen PRRS-Symptome (Shibata et al., 2003; Thacker et al., 1999, Borobia et al., 2014). Pleuritis ist eine der Läsionen, die in der Lunge PRRS-infizierter Tieren auftreten (Muirhead and Alexander, 1997). BPEX (2009) stellte fest, dass die wirtschaftlichen Auswirkungen von Pleuritis beträchtlich waren. Eine zunehmende Prävalenz von Pleuritis wurde mit einem geringeren Schlachtkörpergewicht und einem höheren Alter bei der Schlachtung in Verbindung gebracht. Aufgrund dieser Begleiterscheinungen wurden bei einer typischen Pleuritis mit 10%iger Prävalenz in jeder Partie Kosten in einer Größenordnung von £2,26 pro Schwein für den Erzeuger errechnet.
Die Impfung mit einem modifizierten Lebendimpfstoff gegen PRRS hat sich für die Begrenzung der Auswirkungen des Feldvirus bei Absetzferkeln, wie in diesem klinischen Fall, als nützlich erwiesen (Waddell et al. 2008).






