In der Praxis werden Atemwegserkrankungen bei Schweinen selten durch einen einzigen Erreger verursacht. In der Regel sind mehrere Erreger gleichzeitig beteiligt, was in Verbindung mit unangemessenen Management- und Umweltbedingungen zu dem Prozess führt, der als Porciner Respiratorischer Krankheitskomplex (PRDC) bezeichnet wird.
In den meisten Fällen sind immer die wichtigsten Primärerreger beteiligt, die den Atemtrakt befallen können, wie das Virus des Porcinen Reproduktiven und Respiratorischen Syndroms (PRRSV), das Porcine Circovirus Typ 2 (PCV2), das Schweineinfluenzavirus (SIV) und Mycoplasma hyopneumoniae (Abb. 1). Diese werden von opportunistischen Bakterien begleitet, welche die Primärinfektion ausnutzen, um ihre pathogene Wirkung zu entfalten, wie z. B. Pasteurella multocida, Bordetella bronchiseptica oder Glaesserella parasuis, um nur einige zu nennen.

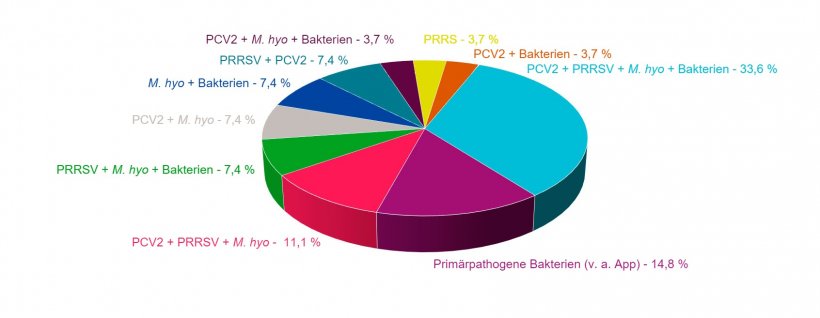
Abbildung 1: Kombinationen von Pathologien bei Fällen von PRDC, die in den letzten vier Jahren vom Dienst für pathologische Anatomie der Veterinärwissenschaftlichen Fakultät der Universität Murcia diagnostiziert wurden.
In Abbildung 1 ist zu sehen, wie M. hyopneumoniae an den meisten Koinfektionen beteiligt ist, die in der Lunge von Tieren festgestellt werden, bei denen man PRDC diagnostizierte. Dieser Krankheitserreger, der die Zilien der Epithelzellen in den Bronchien und Bronchiolen angreift und das mukoziliäre Transportsystem verändert, führt auch zur Hyperplasie des lymphatischen Gewebes, das mit der Schleimhaut der Atemwege assoziiert ist. Beide Vorgänge erleichtern die Besiedlung, Vermehrung und pathogenen Mechanismen anderer Primär- und Sekundärerreger, die den Atemtrakt der Schweine beeinträchtigen. Verschiedene experimentelle Studien haben gezeigt, dass das Bakterium nicht nur die Wirkung anderer Krankheitserreger erleichtert, sondern diese in der Regel auch potenziert, so dass die Kombinationen, in denen M. hyopneumoniae auftritt, in der Regel diejenigen mit den schlimmsten Folgen für die betroffenen Tiere und damit für die Rentabilität des Betriebs sind.
Eine der häufigsten Koinfektionen in Schweinehaltungsbetrieben mit Fällen von PRDC ist eine Koinfektion, die durch M. hyopneumoniae und PRRSV hervorgerufen wird (Abb. 2). In den Fällen, in denen diese Koinfektion diagnostiziert wurde, stellte man eine positive Korrelation zwischen den Tieren fest, die bezüglich jedes einzelnen der beiden Erreger seropositiv sind. Mit anderen Worten: Die meisten Tiere, die PRRSV-positiv sind, sind auch bezüglich M. hyopneumoniae positiv. Darüber hinaus wurde nachgewiesen, dass M. hyopneumoniae die durch PRRSV hervorgerufene Lungenentzündung verlängert und verstärkt, was darauf zurückzuführen sein könnte, dass bei Tieren, die mit beiden Erregern koinfiziert sind, eine Zunahme von pro-inflammatorischen Zytokinen wie IL1-β, IL-8 und TNF-α erfolgt, die die Entzündungsreaktion auf Lungenebene verstärken. Aber es gibt auch eine verstärkte Synthese von IL-10, einem entzündungshemmenden Zytokin, das die Produktion anderer Zytokine hemmt und reguliert und es ermöglichen würde, den Schaden auf Lungenebene aufrechtzuerhalten, indem es die Auslösung einer unkontrollierten Entzündungsreaktion verhindert. IL-10 ist auch in der Lage, die Immunantwort des Tieres zu modulieren, was zusammen mit der Aktivierung anderer Mechanismen die adaptive Immunantwort verändert und es dem Erreger möglich macht, in der Lunge längere Zeit Wirkung zu zeigen.
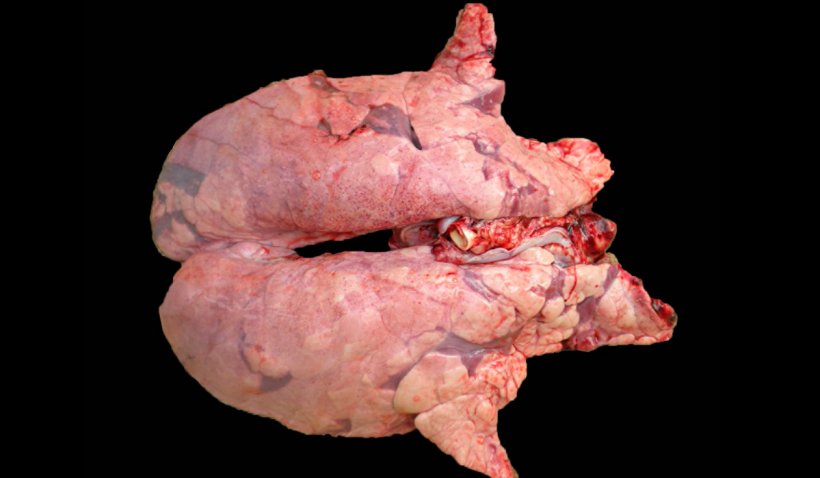
Abbildung 2: Mit M. hyopneumoniae und PRRSV koinfizierte Lunge eines Schweins. Nicht kollabierte Lunge mit rötlich-braunen Bereichen mit Läsionen, die über das Parenchym verteilt sind, typischen PRRS-Läsionen, die gleichzeitig rötliche konsolidierte Stellen in den kranioventralen Bereichen aufweisen, die durch die Infektion mit M. hyopneumoniae hervorgerufen wurden.
Im Falle einer Koinfektion mit M. hyopneumoniae und PCV2 hat sich gezeigt, dass M. hyopneumoniae die Schwere der durch PCV2 hervorgerufenen Läsionen in der Lunge und den lymphatischen Organen mildert und eine stärkere Virusvermehrung sowie seine Persistenz in den Geweben fördert (Abb. 3), wodurch sich die Inzidenz von PCV2-bedingten systemischen Erkrankungen (aktuelle Bezeichnung für PMWS, engl. Postweaning Multisystemic Wasting Syndrome) erhöht.
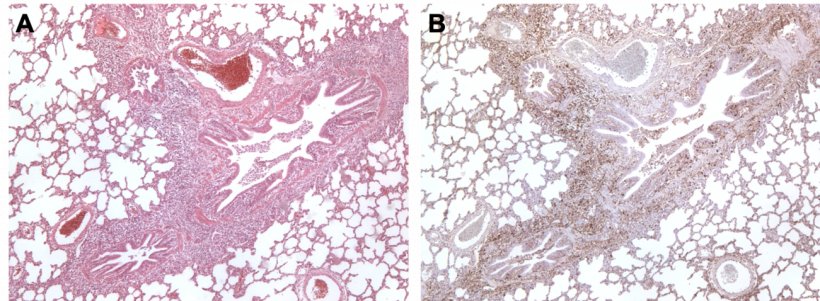
Abbildung 3: Mit M. hyopneumoniae und PCV2 koinfizierte Lunge eines Schweins A: Bereich der peribronchiolären lymphatischen Hyperplasie, verursacht durch M. hyopneumoniae. B: Große Mengen des PCV2-Antigens im Bereich der lymphatischen Hyperplasie.
Bei Tieren mit Koinfektionen von M. hyopneumoniae und SIV (Abb. 4) wurden im Falle einer Infektion von Schweinen mit M. hyopneumoniae, die sich danach mit einem niedrigvirulenten Stamm des Schweineinfluenzavirus infizierten, eine starke Zunahme der klinischen Symptome und Lungenläsionen beobachtet, was darauf hindeutet, dass Mykoplasmen die Virulenz dieser SIV-Stämme erhöhen können.
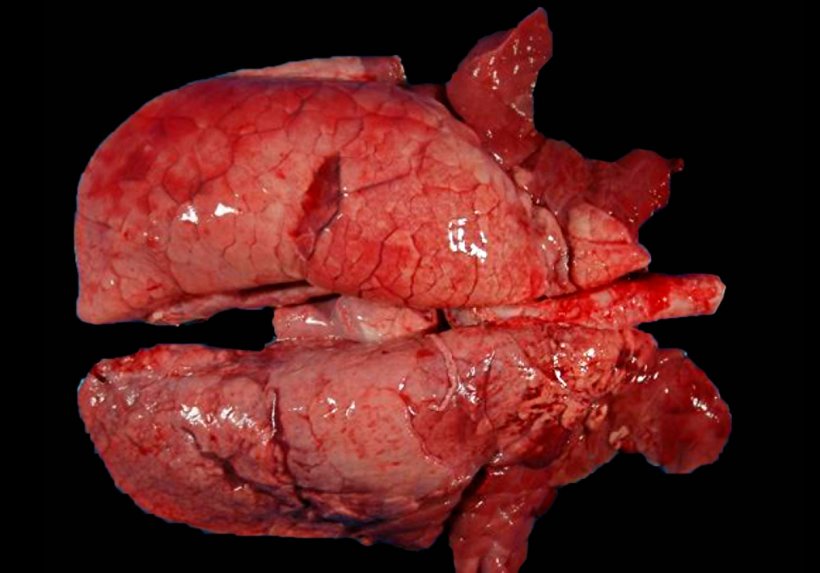
Abbildung 4: Mit M. hyopneumoniae und SIV koinfizierte Lunge eines Schweins. Rote konsolidierte Stellen in den kranioventralen Teilen der Lunge und einige kleinere Bereiche im Zwerchfelllappen. Bei diesen kranioventralen Läsionen gibt es sowohl Läsionen durch M. hyopneumoniae als auch Läsionen aufgrund von SIV, so dass eine makroskopische Unterscheidung zwischen ihnen unmöglich ist.
M. hyopneumoniae scheint auch häufig mit anderen Bakterien assoziiert zu sein, unabhängig davon, ob es sich um Primärerreger wie Actinobacillus pleuropneumoniae (Abb. 5) oder um opportunistische Erreger wie Pasteurella multocida (Abb. 6) handelt, die ihre Wirkung in der Lunge verstärken.
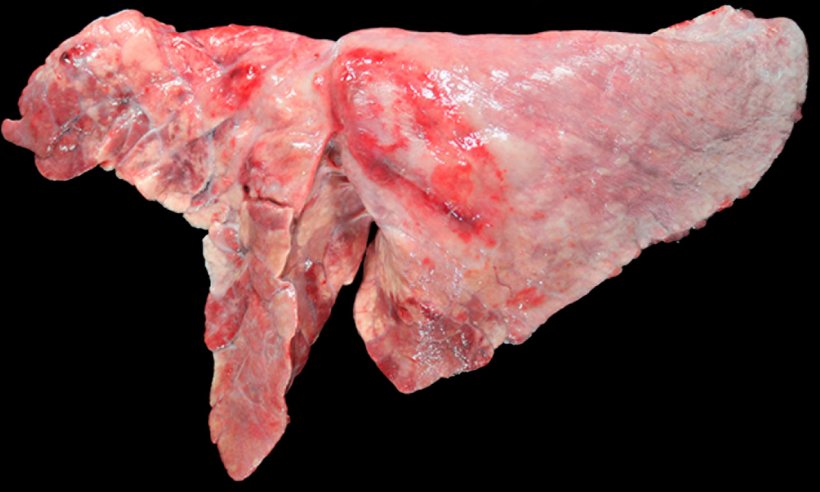
Abbildung 5: Mit M. hyopneumoniae und A. pleuropneumoniae koinfizierte Lunge eines Schweins. Kranioventrale konsolidierte Bereiche mit rötlich-brauner Färbung, verursacht durch eine Infektion mit M. hyopneumoniae, und eine ovalförmige Läsion mit pleuraler Fibrose und hämorrhagischem Bereich im Zwerchfelllappen, was zum chronischen Stadium nach Auftreten einer durch A. pleuropneumoniae verursachten Nekrose passen würde.
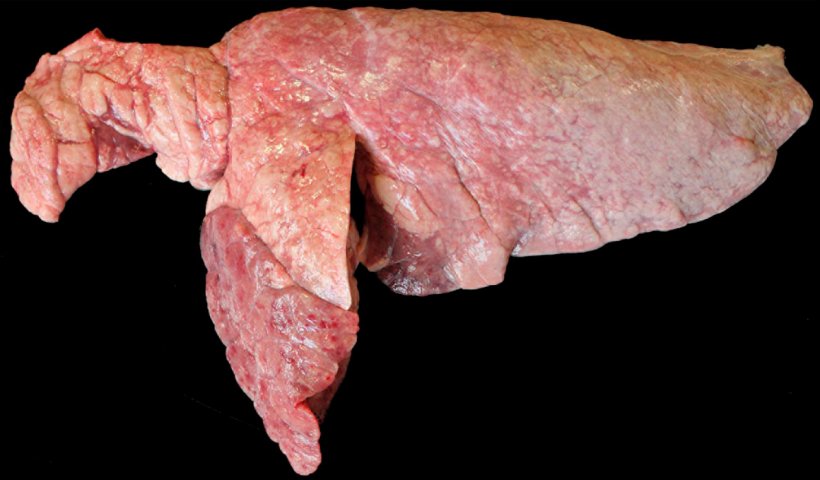
Abbildung 6: Mit M. hyopneumoniae und P. multocida koinfizierte Lunge eines Schweins. Konsolidierte kranioventrale Bereiche mit rötlich-brauner Färbung, die im Vergleich zum restlichen Lungenparenchym erhöht sind, was auf eine durch P. multocida verursachten Läsion hindeuten könnte. Im Oberlappen und am kranioventralen Rand des Unterlappens finden sich rötliche, eingedrückte, konsolidierte Bereiche, die zu einer durch M. hyopneumoniae verursachten Läsion passen.
Wie wir gesehen haben, verstärkt und verlängert M. hyopneumoniae bei Koinfektionen zusammen mit anderen Primärerregern des PRDC die durch diese Erreger verursachten Läsionen, weshalb seine Kontrolle von entscheidender Bedeutung ist, wenn man die Auswirkungen des PRDC minimieren und die mit der Krankheit verbundenen wirtschaftlichen Verluste verringern möchte.






