Wer hat nach einer Tränkwassermedikation nicht schon einmal alle Tränken in einem Aufzuchtstall gesperrt? Wie oft haben wir schon dem für die Behandlung verwendeten Produkt die Schuld gegeben?

Abbildung 1: Salzintoxikation bei Aufzuchtferkeln
Eine Verstopfung der Tränken ist nicht das Schlimmste, was passieren kann, denn wenn dies passiert, wissen wir mindestens, dass die Schweine kein Wasser oder keine Medikamente erhalten haben. Aber manchmal schlägt die Verabreichung von Medikamenten über das Tränkwasser scheinbar ohne Grund fehl. In solchen Situationen kommen Zweifel auf: Wir beginnen am Produkt, an der Dosierung, an dem Mitarbeiter, der die Behandlung durchgeführt hat, oder sogar an der Diagnose zu zweifeln, wenn wir negative Ergebnisse sehen.

Damit ein Molekül wasserlöslich ist, muss es in der Lage sein, sich selbst zu ionisieren. Wenn es keine Radikale besitzt, die zur Ionisierung fähig sind, wird es ausfällen und sich bei der Medikation des Tränkwassers in einem Tank auf dem Boden absetzen. Genau das wird passieren, wenn wir eine „Vormischung“ im Tränkwasser verwenden würden.

Abbildung 2: Beispiel für eine Ausfällung
Ein Molekül, das in der Lage ist, sich selbst zu ionisieren, wenn es mit Wasser in Kontakt kommt, wäre zum Beispiel ein Salz, und dies ist eine der häufigsten Darreichungsformen von löslichen Medikamenten. Ein Salz spaltet sich selbst in zwei Arten von Radikalen auf: in saure (positiv geladene) und in basische (negativ geladene). Nicht alle verwendeten Moleküle spalten sich in die gleiche Menge an sauren und basischen Radikalen auf. Die Eigenschaft, sich in mehr oder weniger saure Radikale aufzuspalten, wird durch die Konstante pKa ausgedrückt. Je kleiner diese Konstante ist, desto saurer ist der molekulare Charakter. So bezeichnet man Moleküle mit einem pKa-Wert von 2,7 (dem von Phenoxymethylpenicillin) als sauer, während sie mit einem pKa-Wert von 7,6 (dem von Lincomycin) als basisch gelten. Wenn der pH-Wert des Mediums, in dem sie gelöst werden, mit ihrem pKa-Wert übereinstimmt, werden die Moleküle zu 50 % ionisiert. Um eine gute Lösung zu erreichen, sollten die Moleküle vollständig ionisiert sein. Somit folgt:
-
Moleküle, die einen schwach basischen Charakter haben, werden in einem sauren pH-Wert (granitisches Wasser) besser ionisiert.
-
Moleküle mit schwach saurem Charakter werden in einem basischen Medium (kalkhaltiges Wasser) besser ionisiert.
Zu den Molekülen, die wir als schwache Säuren einstufen können, gehören Ampicillin, Phenoxymethylpenicillin, Amoxicillin, Chinolon-Antibiotika usw.
Zu den Molekülen, die wir als schwache Basen einstufen können, gehören Makrolide, Lincosamide, Tiamulin, Tetracyclin usw.
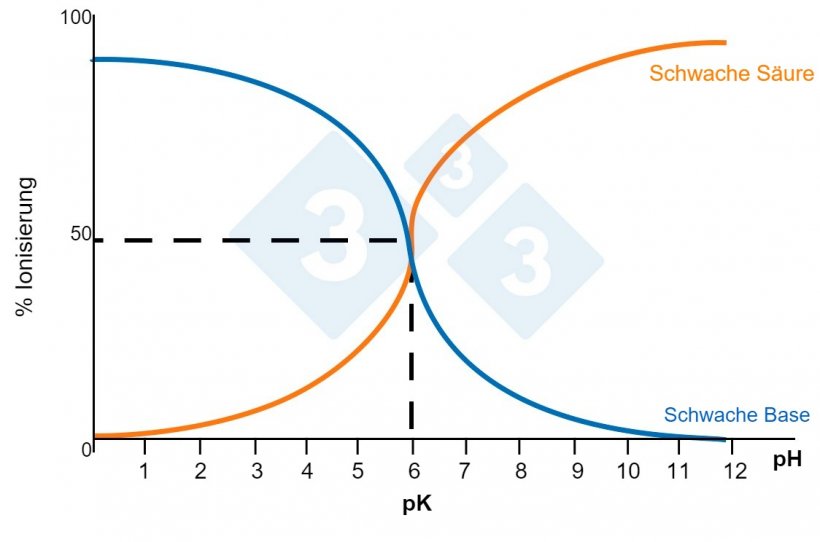
Abbildung 3: Löslichkeit von Verbindungen
In der Praxis kann eine leichte Ansäuerung oder Neutralisierung des Tränkwassers interessant sein, um die Löslichkeit der verwendeten Produkte zu verbessern.
Tipp: Um Probleme mit schwach basischen Molekülen wie Tetracyclin zu vermeiden, empfiehlt sich eine Ansäuerung des Tränkwassers.
Bei Stoffen, die als schwache Säuren eingestuft werden, wie z. B. Amoxicillin, Ampicillin oder Phenoxymethylpenicillin (üblich in frühen Phasen wie nach dem Absetzen), ist es ratsam, sie nicht in angesäuertem Wasser zu verwenden.
Stark angesäuertes Wasser (pH-Wert < 5) könnte sogar die Wirksamkeit dieser Stoffe einschränken und mögliche Folgen dieser Medikamente beeinträchtigen.













