Methoden zum Nachweis von Antikörpern gegen PRRSV
Der indirekte Immunfluoreszenz-Assay (IFA), der Serumneutralisationstest (SVN), der Immunperoxidase Monolayer Assay (IPMA) und der Enzyme Linked Immunosorbent Assay (ELISA) wurden alle für den Nachweis von PRRSV-spezifischen Antikörpern eingesetzt. IFA, SVN und ELISA stehen derzeit in den meisten nordamerikanischen veterinärmedizinischen Diagnoselaboren zur Verfügung, während IPMA in Europa sehr weit verbreitet ist. Alle Tests gelten als spezifisch, weisen aber einen unterschiedlichen Sensivitätsgrad auf. Typischerweise dienen IFA, IPMA und ELISA zum Nachweis der gesamten PRRSV-spezifischen Antikörper der IgG-Klasse, während der SVN-Test zum Nachweis funktioneller Antikörper in Verbindung mit der Immunität oder dem Immunschutz eingesetzt wird. IFA und ELISA wurden angepasst, um andere Isotypen wie z. B. IgM oder IgA (Abb. 1) nachzuweisen. PRRSV-spezifische IgG-Antikörper, die durch IFA, IPMA oder ELISA festgestellt werden können, werden in infizierten Schweinen 7 bis 14 Tage nach der Infektion gebildet, SVN-Antikörper sind jedoch erst 1 bis 2 Monate nach der Infektion (Abb. 2) nachweisbar. Generell können PRRSV-Antikörper, die von einer aktiven Infektion stammen, 3 bis 4 Monate lang nach der Infektion zuverlässig erkannt werden und 6 Monate bis zu 1 Jahr nach dem Ausbruch bestehen bleiben.

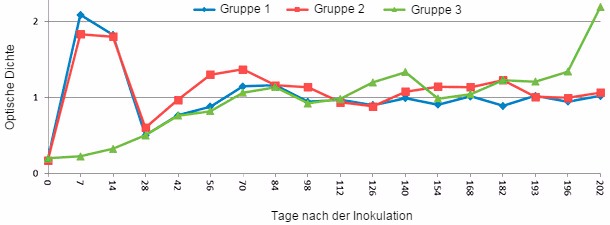
Abbildung 1: IgM-Reaktion bei jungen Schweinen nach experimenteller PRRSV-Infektion, gemessen nach IDEXX PRRS ELISA 2XR mit Änderungen. Gruppe 1 und 2 wurden am Tag 0 mit PRRSV Typ 2 intranasal geimpft. Gruppe 1 wurde im Gegensatz zu Gruppe 2 196 Tage nach der Inokulation (dpi) erneut geimpft. Gruppe 3 wurde erst am 196. Tag nach der Inokulation mit PRRSV geimpft. PRRSV-spezifische IgM-Antikörper sind 7 dpi nachweisbar und nehmen nach 14 dpi schnell ab. (Nezami S und Yoon KJ, unveröffentlichte Daten)
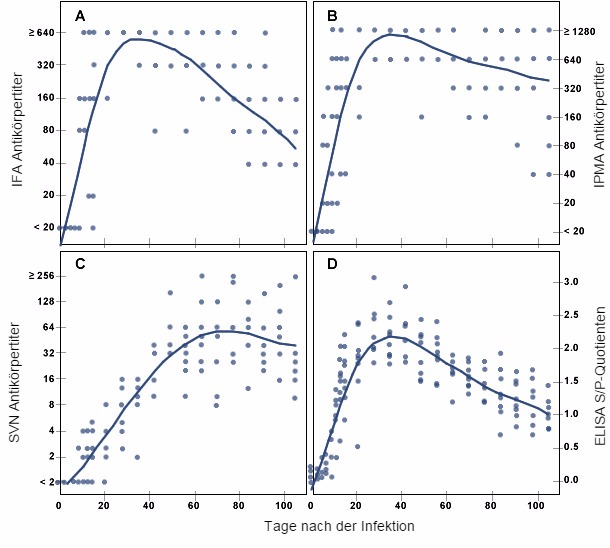
Abbildung 2: PRRSV-spezifische Antikörperreaktion bei Schweinen im Laufe der Zeit nach experimenteller Infektion gemessen durch indirekten Immunfluoreszenz-Assay (A), Immunperoxidase Monolayer Assay (B), Serumneutralisationstest (C) und Enzyme Linked Immunosorbent Assay (D). (Übernommen aus der Publikation von Yoon K-J, et al.: Characterization of the humoral immune response to PRRSV infection. Journal of Veterinary Diagnostic Investigation, 7:305-312, 1995)
In den Testverfahren IFA und IPMA werden virusinfizierte Zellen als Antigen benutzt (Abb. 3). Ein Vorteil dieser Tests im Vergleich zu ELISA ist, dass die Höhe des Antikörpertiters bestimmt werden kann. Die Endpunkte von IFA Antikörpertitern variieren jedoch oft je nach Laborant und Labor, da die Interpretation sehr subjektiv ist. Darüber hinaus variieren Testergebnisse oder Endpunkt-Antikörpertiter je nach dem Grad, zu dem sich der PRRSV-Stamm, der im Assay benutzt wird, antigenisch von dem Isolat unterscheidet, durch das die Infektion beim Schwein hervorgerufen wurde.
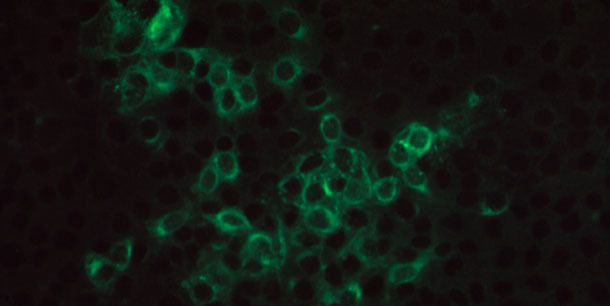
Abbildung 3: Fotomikroskopische Aufnahme positiver Immunofluoreszenz bei einer Monoschicht aus PRRSV-infizierten MARC145-Zellen, die mit einem Schweineserum inkubiert wurde, das PRRSV-spezifische IgG-Antikörper enthielt, und mit FITC-konjugierten Ziegen-Anti-Schwein-IgG-Antikörpern gefärbt wurde.
Es wird angenommen, dass das ELISA-Verfahren sensitiver als IFA und IPMA ist. Es wurden verschiedene ELISA-Formate beschrieben: ein indirektes ELISA-Format, bei dem ein System benutzt wird, welches das Verhältnis der Probe zur Positivkontrolle (S/P-Quotient) berücksichtigt, ein indirektes ELISA-Format, bei dem direkte OD-Werte benutzt werden, und ein Blocking-ELISA. Derzeit gibt es verschiedene handelsübliche ELISA-Kits zum Nachweis von PRRSV-spezifischen Serumantikörpern (Abb. 4). Einheitlichkeit bei der Herstellung des Kits und ein hoher Automatisierungsgrad bei der Durchführung des Tests im Diagnoselabor führen zu weniger Abweichungen der Ergebnisse der im Handel erhältlichen ELISA-Tests im Vergleich zu anderen Assays. Weitere Vorteile des handelsüblichen ELISA-Kits sind: a) der Nachweis von Antikörpern gegen beide PRRSV-Typen, b) kurze Analysezeiten und c) die Lizenzierung. Vor kurzem wurde die ELISA-Plattform auch an die Untersuchung von Proben oraler Flüssigkeit auf PRRSV-Antikörper im Rahmen der Gesundheitsüberwachung im Bestand angepasst.

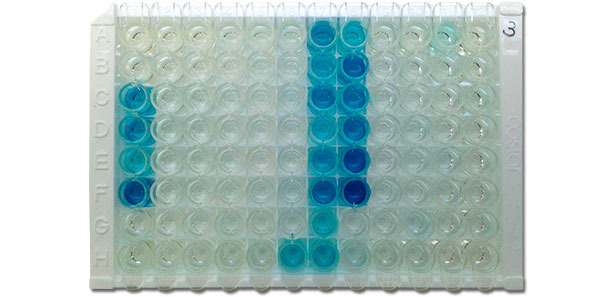
Abbildung 4: Bild einer IDEXX ELISA X3 Platte mit positiven (blaue Farbe) und negativen (keine Farbe) Ergebnissen. Die Farbdichte korreliert mit dem Antikörperspiegel des Serums, d. h. je dunkler die Farbe, desto höher ist der Antikörpertiter. (Foto mit freundlicher Genehmigung von: Dr. David Baum, Veterinärmedizinisches Diagnoselabor der Iowa State University)
Der SVN-Test gilt auch als spezifischer Test, aber frühere Studien legten nahe, dass SVN weniger sensitiv ist als IFA und ELISA. Die geringe Sensitivität des Tests ist vor allem auf die Tatsache zurückzuführen, dass neutralisierende Antikörper gegen PRRSV spät und langsam gebildet werden. Aufgrund des hohen Arbeitsaufwands, mit dem der SVN-Test verbunden ist, sollte dieser eher als eine Forschungsmethode denn als ein routinemäßiger diagnostischer Test betrachtet werden. Wie auch bei IFA und IPMA werden die Testergebnisse stark beeinflusst durch den Grad der antigenischen Verwandtschaft zwischen dem Isolat, das in dem Test benutzt wurde, und dem Isolat, mit dem sich die Schweine infiziert haben.
Interpretation serologischer Befunde in der PRRS-Diagnostik
Serologische Untersuchungen können dazu beitragen, das Vorkommen (also die Seropositivität) und den Status (z. B. hohe Antikörperspiegel bei kürzlichen Infektionen) einer PRRSV-Infektion im Bestand zu bestätigen. Die serologische Information aus einer einzigen Probe reicht für die Diagnose von klinischem PRRS bei einem einzelnen Tier nicht aus, da PRRSV-Infektionen in Schweinebeständen sehr häufig auftreten. Bei der Interpretation serologischer Befunde bei jungen Schweinen sollte das mögliche Vorkommen maternaler Antikörper berücksichtigt werden. Es darf auch nicht vergessen werden, dass die aktuellen serologischen Assays, die bei der Diagnose benutzt werden, Antikörper, die von Impfstoffen stammen, normalerweise nicht von Antikörpern unterscheiden können, die aus Isolaten stammen, die sich unter Feldbedingungen entwickelt haben. Darüber hinaus wurden mutmaßlich falsche PRRSV-positive serologische Befunde festgestellt, die sogar bei handelsüblichen ELISA-Kits auftraten. Außerdem erlauben PRRSV-negative serologische Befunde bei Proben zu einem bestimmten Zeitpunkt verschiedene mögliche Interpretationen: a) Die Schweine waren nicht mit dem Virus infiziert; b) Die Schweine haben sich kürzlich mit dem Virus infiziert und zeigen noch keine Serokonversion; c) Die Schweine waren mit dem Virus infiziert, wurden aber seronegativ; und d) Das Ergebnis war negativ aufgrund der niedrigen Sensitivität des Tests oder eines Laborfehlers. Bei der Entnahme von Einzelproben muss deshalb die PRRS-Serologie in Verbindung mit adäquaten Stichprobenverfahren eingesetzt werden, nicht um festzustellen, ob einzelne Tiere infiziert sind, sondern um festzustellen, ob ein Bestand dem PRRSV ausgesetzt war.
Generell wird empfohlen, lieber junge Schweine als Zuchttiere zu testen, um den PRRSV-Infektionsstatus einer Herde zu bestimmen. In einem Betrieb, in dem alle Altersgruppen vom Ferkel bis zum Endmastschwein an einem Standort gehalten werden, ist die Seroprävalenz der PRRSV-Infektionen im Bestand der Mast- und Endmastschweine normalerweise am höchsten. Das Serum von 10 Endmastschweinen reicht oft aus um festzustellen, ob der Bestand dem PRRSV ausgesetzt war. Bei Multisite-Betrieben repräsentiert jede Produktionsstufe eine einzelne Population, so dass Proben von jedem Standort entnommen werden sollten, und eine Reihe von Blutproben aus verschiedenen Produktionsstufen ist sinnvoll um das Alter zu bestimmen, bei dem eine PRRSV-Infektion am häufigsten auftritt.
Die Serodiagnose einer PRRSV-Infektion als Grund für reproduktive Störungen oder eine Atemwegserkrankung kann durch den Nachweis einer Serokonversion durch Untersuchung gepaarter Serumproben oder durch eine Veränderung beim Antikörpertiter (also Antikörpertiteranstieg) in gepaarten Serumproben erfolgen. Dennoch können Sauen dem Virus 2 oder mehr Wochen vor dem Einsetzen der klinischen Symptome ausgesetzt gewesen sein, in welchem Fall kein Anstieg der Antikörpertiter festzustellen sein könnte. Vorhandene PRRSV-Antikörper in fötalen Flüssigkeiten oder in Blut, das totgeborenen und lebensschwachen Ferkeln vor der Aufnahme der Kolostralmilch entnommen wurde, ist auch ein Zeichen für eine PRRSV-Infektion. Dennoch erfordert eine eindeutige diagnostische Bewertung von PRRS bezüglich der klinischen Erkrankung die Interpretation serologischer Daten zusammen mit Ergebnissen aus anderen Virentests.








