Einleitung
Es handelt sich um einen Zucht- und Mastbetrieb mit 400 Sauen in Nordirland.

Der Betrieb war negativ gegenüber Schweineinfluenza und PRRS (Porcines Reproduktives und Respiratorisches Syndrom).
Die benutzten Impfpläne sind in Tabelle 1 dargestellt.
Tabelle 1: Impfplan
| IMPFSTOFF | JUNGSAUEN | SAUEN | EBER | FERKEL |
| Parvovirus | Injektion von 2 ml bei der Selektion | Injektion von 2 ml 2 Wochen nach dem Abferkeln | ||
| Erysipel | Injektion von 2 ml bei der Selektion und 2 Wochen vor der Deckung | Injektion von 2 ml 2 Wochen nach dem Abferkeln | Injektion von 2 ml zweimal pro Jahr | |
| Colibacillose | Injektion von 2 ml 6 und 2 Wochen vor dem Abferkeln | Injektion von 2 ml 2 Wochen vor dem Abferkeln | ||
| PCV-2 | Injektion von 2 ml 3 Wochen vor der Deckung und 3 Wochen vor dem Abferkeln | Injektion von 2 ml 3 Wochen vor dem Abferkeln | Injektion von 2 ml zweimal pro Jahr | |
| Enzootische Pneumonie | 1 ml im Alter von 7 Tagen und beim Absetzen |
Die Jungsauen wurden im Betrieb selbst gezüchtet. Jungsauen und Sauen wurden mit Samen aus einem einzigen Zuchtbetrieb künstlich besamt.
Verlauf
Der Landwirt kontaktierte den Tierarzt aufgrund des verstärkten Auftretens subkutaner Blutungen und Blutergüsse bei Ferkeln, die aus 8 verschiedenen Würfen stammten. Bisher waren mit dem Auftreten dieser Symptome noch keine Todesfälle verbunden.
In den vergangenen 3 Jahren waren in dem Betrieb die gleichen Symptome aufgetreten, allerdings nicht in demselben Ausmaß wie jetzt. Die klinischen Symptome traten bei einigen Würfen plötzlich auf und verschwanden dann wieder für bestimmte Zeit.
Untersuchung
Klinische Untersuchung
Bei einem Besuch des Betriebs wiesen 28 Ferkel aus 8 verschiedenen Würfen großflächige subepitheliale Blutungen auf (Abbildungen 1, 2, 3, 4 & 5). Die Ferkel wurden normal geboren und entwickelten die klinischen Symptome erst ab dem Alter von 7 Tagen. Die betroffenen Ferkel saugten weiterhin normal und schienen in keiner Weise verkümmert. Nicht alle Ferkel der betroffenen Würfe zeigten äußere klinische Symptome.

Abbildung 1: Kampfspuren und großflächige subepitheliale Blutungen bei 7 Tage alten Ferkeln. 12 Stunden nach dem Kupieren wurde getrocknetes Blut auf den Heizmatten festgestellt. Abbildung 2: Kampfspuren und großflächige subepitheliale Blutungen bei 7 Tage alten Ferkeln. 12 Stunden nach dem Kupieren wurde getrocknetes Blut auf den Heizmatten festgestellt.

Abbildung 3: Kampfspuren und großflächige subepitheliale Blutungen bei einem 7 Tage alten Ferkel

Abbildung 4: Großflächige subepitheliale Blutungen und Bildung von Petechien bei einem 7 Tage alten Ferkel

Abbildung 5: Kampfspuren und großflächige subepitheliale Blutungen bei einem 7 Tage alten Ferkel
Als der Tierarzt den Betrieb besuchte, wurden die Ferkel gerade kupiert. Die Blutung aus dem Schwanz war stark und die Gerinnung verzögert (Abbildungen 1 & 2).
Als man bei 10 betroffenen Ferkeln die Rektaltemperatur maß, wurde kein Fieber festgestellt.
Laboruntersuchungen
Dem Labor wurden ein vor Kurzem verendetes und ein lebendiges, krankes, 7 Tage altes Ferkel übergeben. Zur hämatologischen Untersuchung im Labor wurde eine heparinisierte Blutprobe angefordert. Die Ergebnisse der Laboruntersuchungen sind in Tabelle 2 zusammengefasst.
Da die Blutproben, die im Labor entnommen wurden, geronnen waren, konnten keine hämatologischen und biochemischen Untersuchungen durchgeführt werden.
Abbildungen 6, 7, 8 & 9 zeigen fotografische Nachweise nach der Obduktion.
Tabelle 2: Laborergebnisse von den beiden 7 Tage alten Ferkeln
| Sektion | Histologie | Immunofluoreszenz | Bakteriologie | |
| FERKEL 1 (tot) | • Großflächige oberflächliche subepitheliale Blutungen mit Bildung von Petechien im Tierkadaver • Blut dünn und wässrig • Einige petechiale Blutungen im Herzen • Blasse Niere mit petechialen Blutungen • Blasse Leber und Gelbsucht |
• Keine auffälligen Anomalien festgestellt. |
• KSPV -und PCV-2-negativ |
• Keine auffälligen Bakterien nachgewiesen |
| FERKEL 2 (lebend) | • Großflächige subepitheliale Blutungen im Tierkadaver • Blut dünn und wässrig • Petechiale Blutungen in Niere und Lunge. |
• Keine auffälligen Anomalien festgestellt |
• KSPV- und PCV-2-negativ. |
• Keine auffälligen Bakterien nachgewiesen |
KSPV = Virus der Klassischen Schweinepest
PCV-2 = Porcines Circovirus Typ 2

Abbildung 6: 7 Tage altes Ferkel: Hervorzuheben sind der blasse Tierkadaver und die großflächigen petechialen Blutungen in der Haut. Die Leber zeigt Gelbsucht. Alle Lymphknoten haben ein hämorrhagisches Erscheinungsbild.

Abbildung 7: Das Herz des Ferkels von Abb. 3: Hervorzuheben sind petechiale Blutungen im Herzen und hämorrhagische Lymphknoten.
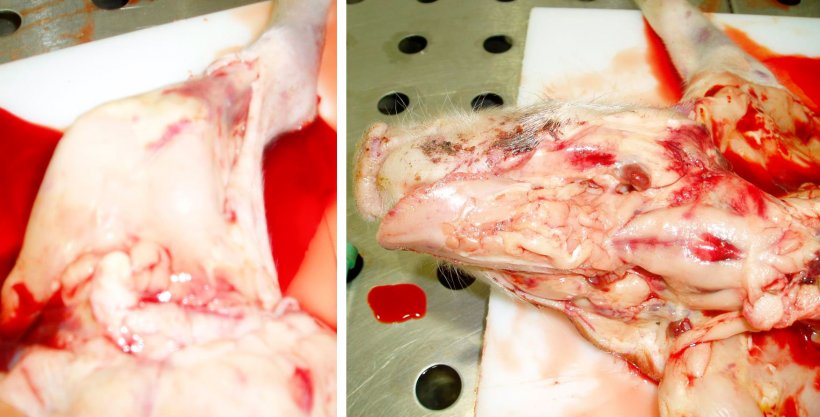
Abbildung 8: Blasser Tierkadaver und subepitheliale Blutungen im linken Hinterbein: Hervorzuheben ist das dünne und wässrige Blut auf dem Tisch. Abbildung 9: Blasser Tierkadaver mit hämorrhagischen Lymphknoten und subepithelialen Blutungen: Hervorzuheben ist das dünne und wässrige Blut auf dem Tierkadaver.
Differentialdiagnose
Auf Grundlage der klinischen Untersuchungen und der Laboruntersuchungen wurde die folgende Liste der Differentialdiagnosen erstellt:
- Thrombozytopenische Purpura
- Eisenmangel
- Vitamin-K-Mangel (Rodentizidvergiftung)
- Klassische Schweinepest (KSPV)
- Porzine Circovirose (PCV-2)
Virale Krankheitserreger wie z. B. KSPV und PCV-2 wurden aufgrund mangelnder klinischer Symptome, die zu diesen Krankheiten passen, und negativer Immunofluoreszenz-Testergebnisse ausgeschlossen.
Eisenmangel wurde aufgrund routinemäßiger Eisen-Dextran-Injektionen, die allen Ferkeln im Alter von 2 Tagen intramuskulär verabreicht wurden, und aufgrund der großflächigen subepithelialen Blutungen ausgeschlossen.
Ein Vitamin-K-Mangel (Rodentizidvergiftung) konnte bei der Differentialdiagnose ohne hämatologische Untersuchung nicht ausgeschlossen werden. Gemäß Punkt 4.2. war die entnommene Blutprobe geronnen, weswegen man keine hämatologische/ biochemische Untersuchung durchführen konnte. In den Abferkelställen wurde allerdings kein Rattengift ausgelegt.
Aufgrund der Krankengeschichte und der einheitlichen Ergebnisse der klinischen Untersuchungen und Laboruntersuchungen liegt die Diagnose thrombozytopenischer Purpura nahe.
Programm zur Bekämpfung
Die betroffenen Würfe wurden von anderen Sauen in Fremdpflege aufgezogen.
Man empfahl, Sauen, die kranke Würfe zur Welt brachten, zu keulen oder sie von einem anderen Eber decken zu lassen.
Reaktion auf das Programm zur Bekämpfung
Einige der betroffenen Ferkel, die in Fremdpflege aufgezogen wurden, starben innerhalb weniger Tage.
Seither wurden vom Betriebsinhaber aber keine weiteren Fälle beschrieben.
Diskussion
Die thrombozytopenische Purpura ist eine Hypersensibilität vom Typ II (oder ein zytotoxischer Typ der Hypersensibilität), bei der Antikörper gegen die Thrombozyten gebildet werden. Dies führt zu ihrer Depletion und zur hämorrhagischen Diathese als damit einhergehende klinische Symptome. Diese Antikörper können nach Bluttransfusionen, durch den Einsatz von Impfstoffen, die Blutprodukte enthalten, oder bei Altsauen entstehen, die Antikörper gegen die Alloantigene bilden, die dem Vatertier und dem Fötus gemeinsam sind. Im letzteren Fall würde man nicht erwarten, dass klinische Symptome bei der Sau auftreten, da sie nur Antikörper gegen allotypische Oberflächenantigene produzieren würde, die nicht in ihren Zellen zu finden sind (Straw et al., 1999). Im Gegensatz zu Menschen und Hundewelpen werden von der Sau vor der Geburt über die Plazenta keine Antikörper auf ihre Ferkel übertragen. Ferkel werden als schutzlose Wesen ohne humorale oder mukosal assoziierte Antikörper geboren und haben keine zellvermittelte Immunität erworben (Muirhead et al., 1997a). Dies würde erklären, warum die Trächtigkeit nicht unterbunden wird. Die Aufnahme dieser Antikörper mit der Kolostralmilch und deren Absorption durch die Ferkel führt zu einem Sinken der Konzentration zirkulierender Thrombozyten auf ca. 200x109/l im Alter von 2 Tagen (normalerweise höhere Konzentration von 250 – 300x109/l). Im Alter von 5 Tagen wird mit 400x109/l wieder eine normale Konzentration erreicht. Und wenn Purpura auftritt, fallen die Werte ab dem Alter von 9 Tagen auf 50x109/l ab. Betroffen sind Megakaryozyten und andere Zellen im Knochenmark und die zirkulierenden Thrombozyten werden nicht ersetzt (Taylor, 1995).
Bluttransfusionen und Impfstoffe, die Blutprodukte enthalten, wie z. B. Kristallviolett-Impfstoff gegen das Schweinefieber (Smith et al., 1990), wurden in diesem Betrieb nicht benutzt. Die einzige Möglichkeit, die dann noch übrig blieb, waren Altsauen, die Antikörper gegen die Alloantigene gebildet hatten, die dem Vatertier und dem Fötus gemeinsam waren. Betroffene Würfe kamen von einem Large White Eber. Alle Sauen, die einen betroffenen Wurf zur Welt brachten, haben zuvor schon mindestens einmal geferkelt. Gemäß Taylor (1995) muss sich, damit die Krankheit auftreten kann, die Thrombozytenart des Ebers von derjenigen der Sau unterscheiden und die Sau muss mindestens einmal zuvor einen Wurf mit einem Eber zur Welt gebracht haben, der diese Art von Thrombozyten besaß. Es stellte sich in unserem Fall heraus, dass die betroffenen Sauen vor einem früheren Wurf von diesem Eber künstlich besamt wurden. Taylor (1995) stellte fest, dass dieses Problem am häufigsten bei Large White und Landrasse-Schweinen auftritt und insbesondere dann weitverbreitet ist, wenn eine Landrasse-Sau von einem Large White Eber gedeckt wird. In diesem Fall erfolgte die künstliche Besamung durch einen Large White Eber und die gedeckten Sauen waren reine Landrassen oder eine Kreuzung aus Landrasse x Large White. Aus diesem Grund empfahl man eine Änderung der künstlichen Besamung, woraufhin sich die Situation verbesserte, ohne dass es notwendig war, die Sauen oder den Eber zu keulen. Leider konnten die Thrombozyten nicht untersucht werden, da die im Labor entnommenen Blutproben geronnen waren. Eine andere Alternative wäre die Blutentnahme im Betrieb gewesen. Seither sind jedoch keine weiteren Krankheitsfälle mehr aufgetreten.
Nicht alle Ferkel der betroffenen Würfe zeigten klinische Symptome. Gemäß Straw et al. (1999) und Taylor (1995) scheint der Zufallseffekt beim Vorliegen der entsprechenden Voraussetzungen in einem Wurf an das Wachstum und die Aufnahme von Kolostralmilch gebunden zu sein, wobei gut entwickelte Ferkel, die mehr Kolostralmilch getrunken haben, stärker betroffen sind. Dies traf auch auf diese Ferkel zu, da alle erkrankten Tiere in gutem körperlichen Zustand und gut entwickelt waren und ihren Appetit nicht verloren hatten.
Von der Krankheit betroffene Schweine erschienen bei der Geburt normal (Straw et al., 1999). Verschiedene Autoren haben von unterschiedlichen zeitlichen Verläufen beim ersten Auftreten der Krankheit berichtet. Danach erschien sie im Alter von 7 – 21 Tagen (Muirhead et al., 1997b), im Alter von 10 – 20 Tagen (Straw et al., 1999) oder im Alter von 14 – 30 Tagen mit einem kleineren Höhepunkt im Alter von 3 Tagen (Taylor, 1995). In diesem Fall trat die Krankheit im Alter von 7 Tagen auf, wie Muirhead et al. (1997b) feststellten.
Todesfälle können ohne klinische Symptome auftreten, wobei sich unter den toten Tieren Schweine finden, die in gutem Zustand erscheinen (Muirhead et al., 1997b; Taylor, 1995). Wenn man die Haut dieser toten Schweine näher betrachtet, sollten überall da Blutungen zu sehen sein, wo es Prellungen, Zahnabdrücke oder Verletzungen gab (Muirhead et al., 1997b). In diesem Fall war es nicht möglich, plötzliche Todesfälle zuzuordnen, die durch thrombozytopenische Purpura und andere Todesursachen, wie z. B. Erdrücken verursacht wurden. Erkrankte Ferkel sind jedoch häufig blass und möglicherweise sind eine fleckige, violette Haut, Blutungen, die sich hauptsächlich am Bauch befinden, und starke Kratzspuren zu sehen. Die Schleimhäute sind normalerweise blass und es tritt kein Fieber auf (Straw et al., 1999; Taylor, 1995). Im Epikard und Myokard, der Pleura, den Gelenken und der Skelettmuskulatur sind Blutungen unterschiedlicher Größe zu beobachten. Alle Lymphknoten sind voller Blut (Muirhead et al., 1997b; Taylor, 1995). All diese Merkmale passten zum Krankheitsbild, das in diesem Fall festgestellt wurde.
Die Kastration während des Auftretens von thrombozytopenischer Purpura kann die Mortalität erheblich steigern (Straw et al., 1999). In diesem Betrieb erfolgte keine Kastration. Dennoch gab es starke Blutungen und die Blutgerinnung nach dem Kupieren war verzögert, wie in der klinischen Untersuchung festgestellt wurde.
Laut Taylor, 1995, liegt die Inzidenzrate dieses Symptoms unter 1%.
Die Diagnose erfolgt durch das charakteristische klinische Krankheitsbild und die Obduktionsergebnisse (Muirhead et al., 1997b; Taylor, 1995). Die Diagnose kann durch die Thrombozytenzahl bestätigt werden (Taylor, 1995). All diese Verfahren wurden durchgeführt. Die Thrombozytenzahl konnte jedoch aus den bei den Laboruntersuchungen genannten Gründen nicht ermittelt werden.
Abgesehen von guten Saugbedingungen sind keine weiteren Verfahren bekannt (Muirhead et al., 1997b; Taylor, 1995). Es wurde nicht über den Einsatz von Vitamin K berichtet (Taylor, 1995), aber es wäre interessant, dies bei künftigen Ausbrüchen zu testen. In den frühen Stadien der Erkrankung lohnt sich die Fremdpflege der Würfe, um den Kontakt mit jeglichen in der Sauenmilch verbleibenden Antikörpern zu vermeiden (Muirhead et al., 1997b), so wie es in diesem Fall gemacht wurde. Ebenso kann eine künstliche Fütterung erfolgen (Taylor, 1995). Die Mortalität ist jedoch sehr hoch.
Die thrombozytopenische Purpura wurde bei anderen Tierarten wie z. B. Rindern und Schafen infolge von Vergiftungen mit Farnkraut beschrieben (Barlow, R., 1983). Menschen bekommen diese Krankheit infolge von infektiösen, autoimmunen, bösartigen oder idiopathischen Erkrankungen (Wei, A. et al., 2007).
Wenn eine Sau solch einen Wurf zur Welt gebracht hat, sollte man sie keulen oder beim nächsten Mal mit einem anderen Eber decken (Muirhead et al., 1997b; Taylor, 1995). Der Betrieb entschied sich statt der Keulung für die Paarung der betroffenen Sauen mit einem anderen Eber. Diese Maßnahme schien erfolgreich gewesen zu sein, da seither keine weiteren Fälle von thrombozytopenischer Purpura gemeldet wurden.







