Einleitung
Bis Anfang des vergangenen Jahres ging man davon aus, dass die Vesikuläre Schweinekrankheit (SVD) von einem der folgenden 4 RNA-Viren hervorgerufen werden würde: Maul-und-Klauenseuche-Virus (MKSV, Aphthovirus aus der Familie der Picornaviridae), Vesikuläres Stomatitis-Virus (VSIV, auch bekannt als VSV, Vesiculovirus der Familie der Rhabdoviridae), Porcines Vesikulärexanthem-Virus (VESV, Vesivirus der Familie der Caliciviridae) oder Virus der Vesikulären Schweinekrankheit (SVDV, Enterovirus der Familie der Picornaviridae). Im vorliegenden Fallbericht werde ich diese Viren als die „großen 4” Viren bezeichnen.

Es gab jedoch sporadische, weltweit (einschließlich Neuseeland, Italien, USA, Brasilien) auftretende Fälle, in denen von der Vesikulären Schweinekrankheit in Beständen berichtet wurde, die sich gegenüber den großen 4 Viren als negativ erwiesen. In einigen Fällen wurde vom Senecavirus A (SVA) in Schweinebeständen berichtet, die an SVD erkrankt waren, bei denen die großen 4 Viren aber nicht nachgewiesen werden konnten. Diese Fälle wurden als „idiopathische Vesikuläre Schweinekrankheit” bezeichnet, da der kausale Zusammenhang zwischen SVA und SVD unklar war.
SVA ist ein RNA-Virus, das (zusammen mit MKSV und SVDV) zur Familie der Picornaviridae gehört. Es war früher als Seneca-Valley-Virus bekannt. SVA ist in der humanmedizinischen Literatur aufgrund seiner onkolytischen Eigenschaften bekannt. Tatsächlich gibt es laufende klinische Studien mit SVA beim Menschen als mögliche Krebstherapie. Es ist bekannt, dass sich SVA bei Schweinen, Rindern und Nagetieren reproduzieren kann. Kürzlich wurde von zwei klinischen Fällen berichtet, die in Verbindung mit SVA bei Schweinen stehen: ein vorübergehender epidemischer Anstieg der neonatalen Mortalität (ETNL) und die Vesikuläre Schweinekrankheit.
Ziel dieser Studie ist es, den klinischen Ausbruch von SVD in Verbindung mit dem Nachweis von SVA zu beschreiben.
Fall
Der Betrieb: Ein Aufzucht- und Mastbetrieb mit 8.000 Sauen im Südosten Brasiliens, zu dem mehrere natürlich belüftete Ställe gehören. Jungsauen zur Remontierung wurden im eigenen Betrieb erzeugt. Sperma wurde von Ebern aus einem externen Zuchtbetrieb bezogen und dreimal pro Woche (Montag, Mittwoch und Freitag) an diesen Betrieb geliefert. Das Betriebspersonal arbeitete nur in diesem Betrieb und die Anlagen/ Einrichtungen wurden nicht mit anderen Betrieben geteilt. Insgesamt gab es in dem Betrieb umfangreiche Biosicherheitsmaßnahmen (Dekontaminierungsraum und Leerzeiten, Abbrausen beim Betreten und Verlassen, relativ seltener Transport der Schweine, Waschen und chemische Desinfektion der Fahrzeuge für den Schweinetransport und 24 Std. Trocknen vor dem Beladen mit Schweinen, Region mit niedriger Schweinebesatzdichte). In diesem Betrieb gab es in den 10 Jahren seines Bestehens keine SVD. Er war PRRSV-negativ und Mykoplasma hyopneumoniae-positiv. In den Mastställen befanden sich 30 Schweine und in den Aufzuchtställen 60 Schweine pro Pferch.
Ausbruch der klinischen Erkrankung:
Tage 1-3: Das Betriebspersonal bemerkte, dass Mastschweine weniger aktiv waren als normalerweise, meldeten dies aber nicht dem Betriebstierarzt. Es wurden keine Läsionen oder Lahmheit festgestellt oder gemeldet
Tage 4-10: Ca. 25% der Schweine der Mast und 15% der Zucht lahmten. Am Tag 9 wurde der Betriebstierarzt kontaktiert, der den Betrieb am Tag 10 besuchte und den Verdacht auf Mykoplasma hyosynoviae äußerte. Beim Besuch des Betriebs erfolgte eine eingehende klinische Untersuchung bei Schweinen aller Altersgruppen. Die Veterinäre entdeckten bei den meisten lahmen Schweinen (>90% der lahmen Schweine) in den Mastställen und bei einigen lahmen Schweinen im Aufzuchtstall (~ 30%) Läsionen im Zwischenklauenspalt und am Fußballen und geringfügige Läsionen am Kronenrand des Hufs.
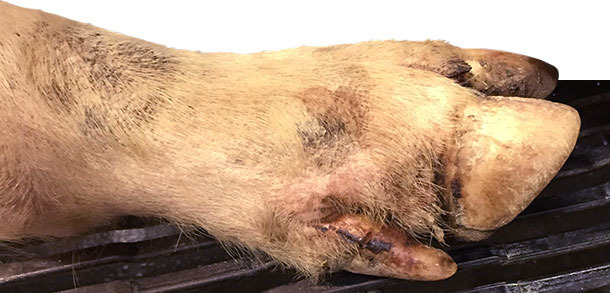
Ebenso fanden sich an den Schnauzen der Mastschweine Bläschen von 0,5 bis 1,5 cm Durchmesser bei ca. 1% der Tiere (ca. ein Schwein von ~ 3 Pferchen). Bei den Ferkeln wurden dagegen nur 2 Bläschen an den Schnauzen gefunden.
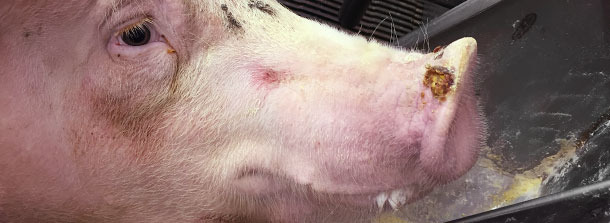
Der Betriebstierarzt benachrichtigte den Amtstierarzt und leitete eine Untersuchung mit Verdacht auf eine fremde Tierkrankheit ein. Von einigen Schweinen wurden Bläschenflüssigkeit und Abstriche des Kronenrands entnommen und dem amtlichen veterinärmedizinischen Diagnoselabor übergeben. Nach 3 Tagen lag der Befund vor, der bezüglich der großen 4 Viren negativ war. Alle Proben wurden durch RT-PCR positiv auf SVA-RNA getestet. Serologische Tests zur Überprüfung des Bestands gab es zu diesem Zeitpunkt nicht (Herbst 2014).
Die Schweine wurden unterdessen weiterhin täglich auf die Entwicklung und/oder das Verschwinden der klinischen Symptome beobachtet, die mit SVD einhergehen. In den Zuchtbeständen (Sauen) wurden keine Lahmheit oder SVD festgestellt. Neonatale Ferkel zeigten ca. 7 Tage lang einen vorübergehenden Anstieg der Mortalität. Die Mortalität kehrte allerdings vom Höchststand, der in der betroffenen Altersgruppe bei 50% lag, zu den Ausgangswerten zurück und SVD wurde weder bei den Sauen noch bei den Ferkeln festgestellt.
Bei den Zucht- und Mastschweinen traten in den 4 Monaten nach dem Auftreten der ersten klinischen Krankheitsanzeichen immer wieder neue Fälle von Lahmheit und schwach ausgeprägter SVD mit einer Inzidenzrate von ca. 5% pro Woche auf.
Wenn Schweine die ersten Anzeichen von Lahmheit zeigten, wurden sie farblich gekennzeichnet und täglich auf klinische Symptome untersucht. SVD machte sich bei den meisten Schweinen entweder vom Tag 0 an oder nach 1-2 Tagen als Lahmheit bemerkbar. SVD-Läsionen waren innerhalb von 7-10 Tagen vollständig ausgeheilt. In der Wachstumsphase der Schweine änderte sich die Mortalitätsrate nicht wesentlich.
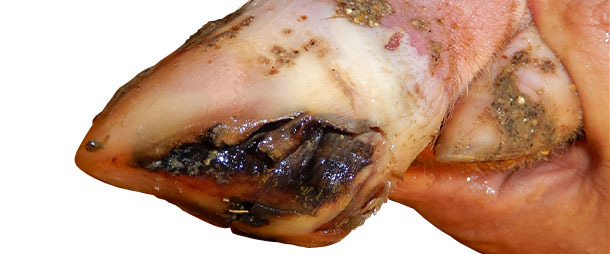
Zwischen 4 und 5 Monaten nach dem Auftreten der ersten Krankheitszeichen sank die Inzidenzrate von SVD-ähnlichen Läsionen auf fast Null. Zum jetzigen Zeitpunkt gibt es im Betrieb seit 6 Monaten keine SVD oder vermehrten Fälle von Lahmheit. Die Behandlung erkrankter Schweine hing von der Schwere der SVD Läsionen ab. Schweine mit schweren Läsionen erhielten eine grundlegende Klauenpflege um ihre Genesung zu unterstützen. Einzelne Schweine mit schwereren Läsionen erhielten intravenös Antibiotika und entzündungshemmende Mittel, um Komplikationen aufgrund sekundärer bakterieller Infektionen zu vermeiden.
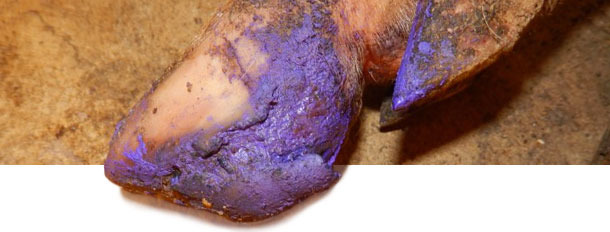
Abschließende Stellungnahme
Vor kurzem wurde auf der ISU Swine Disease Conference in Ames, Iowa, USA, von einer Studie berichtet, die von der Iowa State University (ISU) zusammen mit dem Landwirtschaftsministerium der Vereinigten Staaten (USDA) durchgeführt worden war. Darin gibt es Hinweise auf SVD, die von SVA-Isolaten aus kommerziellen Schweinebetrieben mit klinischer SVD hervorgerufen wurde. Deshalb kann SVA ab sofort neben den großen 4 als einer der ätiologischen Krankheitserreger von SVD bei Schweinen betrachtet werden (jetzt die großen 5).
Obwohl SVD, die durch SVA hervorgerufen wird, im Vergleich zu MKSV schwach bis leicht ausgeprägt und vorübergehend ist, ist die anfängliche Entwicklung der SVD-Läsionen klinisch nicht von den durch MKSV verursachten Symptomen zu unterscheiden. Die Diagnose muss von Amtstierärzten durchgeführt werden um MKSV auszuschließen und die Erkrankungen dürfen nicht mit der Annahme abgetan werden, dass „dies ein weiterer SVA-Fall ist”, wenn man weiß, dass SVA zirkuliert und in nahegelegenen Schweinebeständen zu SVD führt.
In diesem speziellen Fall konnte die Quelle der Einschleppung des Virus nicht bestätigt werden. Es war bekannt, dass andere Betriebe in der Region von einem SVA-assoziierten vorübergehenden epidemischen Anstieg der neonatalen Mortalität und/oder SVD-Läsionen (mindestens 8 Betriebe im Umkreis von 10 km) berichtet hatten. Man stellte auch Vermutungen über Stechmücken (andere Picornaviren werden bekanntermaßen durch Vektoren übertragen), Aerosole, Futtermittelbestandteile, Impfstoffe und Fahrzeuge für den Schweinetransport als mögliche Krankheitsursache an.
Dieser Fall war ein hervorragendes Beispiel dafür, dass unerwartete Krankheitserreger jederzeit auftreten können. Biosicherheitsmaßnahmen sollten deshalb immer überprüft und täglich (stündlich) strikt umgesetzt werden.







